Mascherine Certificate CE, NON marcate CE e filtranti, cerchiamo di capire le differenze.
Per fronteggiare l’emergenza Coronavirus, l’uso di mascherine è diventato importantissimo per proteggere se stessi e gli altri. Vista l’ingente richiesta di questi mezzi di protezione, il Decreto Cura Italia (d.l. 18/2020) ha adottato misure straordinarie che adottano deroghe temporanee alle direttive europee che regolamentano la commercializzazione di Dispositivi di Protezione Individuale (DPI) o Dispositivi Medici (DM), offrendo alla popolazione la possibilità di utilizzare altri tipi di mascherine.
Il risultato è che oggi si trovano in commercio diversi tipi di maschere facciali, vediamo quali sono e quando ne è consentito l’uso.
| Mascherine Chirurgiche | 
|
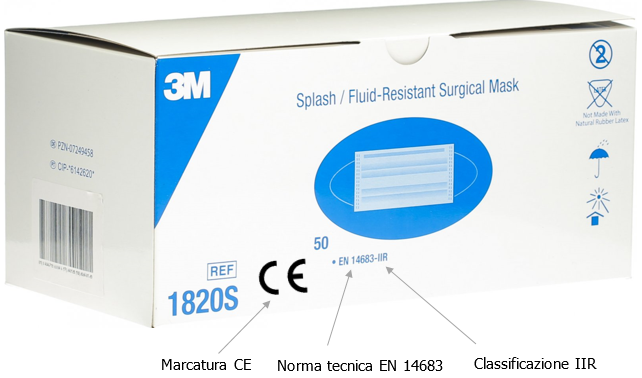
Le mascherine chirurgiche sono dei dispositivi medici secondo il D.Lgs. 24 febbraio 1997, n.46 e s.m.i. (l’entrata in vigore del Regolamento UE 201/745 sui dispositivi medici è stata rinviata al maggio 2021) e come tali, devono essere certificati con marcatura CE
La norma tecnica di riferimento per la loro produzione è la UNI EN 14683:2019. In particolare la norma tecnica indica i requisiti di:
È consentito fare ricorso alle mascherine chirurgiche quali DPI idonei a proteggere gli operatori sanitari (art. 34, comma 3, d.l. 9/2020). Inoltre, le mascherine chirurgiche sono considerati DPI per i lavoratori che sono oggettivamente impossibilitati a mantenere la distanza interpersonale di 1 metro (art. 16, comma 1, d.l. 18/2020, il cd. Decreto Cura Italia). Le mascherine chirurgiche evitano che chi le indossa contamini l’ambiente. La mascherina DEVE essere dotata di Marchio CE, riferimento alla norma |
| Mascherine FFP2 e FFP3 |  |
Le mascherine FFP2 e FFP3, chiamate anche facciali filtranti, sono dispositivi di protezione individuale (DPI) secondo il D.Lgs. 475/1992, ora adeguato con D.Lgs. 17/2019 al Regolamento UE 425/2016 e come tali, devono essere certificati con marcatura CE. La Mascherina DEVE essere dotata di Marchio CE, seguita dal nome o numero identificativo dell’Organismo notificato che ha verificato il dispositivo e da un pittogramma del rischio che il DPI è destinato a contenere. Le maschere sono distinte quindi nelle tre categorie FFP1, FFP2 e FFP3 in base all’efficienza filtrante e alla perdita di tenuta; e in riutilizzabili (indicate con R) o utilizzabili solo per un singolo turno di lavoro (indicate con NR). Se poi hanno superato una ‘prova di intasamento’ riportano anche la lettera D (dolomite).
La norma tecnica di riferimento per la loro produzione è la UNI EN 149:2009. In particolare la norma tecnica indica i requisiti di: La norma tecnica individua i requisiti minimi:
I dpi FFP2 e FFP3 possono essere dotate di valvola o meno:
|
| Mascherine chirurgiche non marcate CE commercializzate come Dispositivi Medici ai sensi dell’ art. 15, comma 2, del D.L. 18/2020 |  |
Sono mascherine ad uso medico, quindi DM, prodotti, importati o messi in commercio, in deroga alle norme comunitarie vigenti, quindi privi della marcatura CE, previo parere favorevole dell’Istituto Superiore di Sanità (ISS).
È infatti prevista una procedura semplificata di validazione straordinaria, per cui il soggetto proponente deve inviare all’ISS un’autocertificazione nella quale, sotto la propria esclusiva responsabilità, attesta le caratteristiche tecniche delle mascherine e dichiara che le stesse rispettano tutti i requisiti di sicurezza di cui alla vigente normativa, nonché trasmettere ogni elemento utile alla validazione delle stesse. L’ISS nel termine di 3 giorni si pronuncia sulla rispondenza delle mascherine chirurgiche alle norme vigenti (art. 15, comma 2, Decreto Cura Italia). |
| Mascherine filtranti non marcate CE commercializzate come Dispositivi di Protezione individuale ai sensi dell’ art. 15, comma 3, del D.L. 18/2020 |  |
Sono DPI prodotti, importati o messi in commercio, in deroga alle norme comunitarie vigenti, quindi privi della marcatura CE, previo parere favorevole dell’INAIL come stabilito dall’art. 15, comma 3, del D.L. 18/2020.
È prevista una procedura di validazione in deroga, analoga a quella prevista per le mascherine chirurgiche, il cui ente competente è però l’lNAIL. |
| Mascherine filtranti senza non marcate CE commercializzate ai sensi dell’ art. 16, comma 2, del D.L. 18/2020 |  |
Non è un DM, né un DPI, ma una mascherina filtrante priva del marchio CE, prodotta in deroga alle norme vigenti sull’immissione in commercio, che può essere prodotta ai sensi dell’art. 16, comma 2, del Decreto Cura Italia.
Il Ministero della Salute ha chiarito che l’art.16 consente a “tutti gli individui presenti sul territorio nazionale, a cui è comunque richiesto di rispettare le disposizioni in tema di distanziamento sociale e le altre regole precauzionali introdotte in ragione dell’emergenza Covid-19, di utilizzare, a scopo precauzionale, mascherine filtranti che per la loro destinazione non si configurano né come DM, né come DPI” (Circolare n. 3572/2020). Queste mascherine non sono soggette ad alcuna procedura semplificata di validazione ed autorizzazione dell’ISS e non devono essere conformi a particolari norme tecniche armonizzate UNI EN – ISO. Possono essere prodotte sotto la responsabilità del produttore che deve comunque garantire la sicurezza del prodotto. Nella citata Circolare è infatti sottolineato che è necessario che i produttori delle mascherine filtranti per la collettività “garantiscano che le stesse non arrechino danni o determinino rischi aggiuntivi per gli utilizzatori secondo la destinazione d’uso prevista dai produttori”. Inoltre, non possono essere utilizzate durante il servizio dagli operatori sanitari né dagli altri lavoratori per i quali è prescritto l’uso di specifici dispositivi di sicurezza. L’imballaggio (o l’etichetta) dovranno quanto meno chiarire che si tratta di una mascherina filtrante prodotta ai fini dell’art. 16, comma 2, d.l. 18/2020, che non è un DM né un DPI, e che ne è escluso l’uso sanitario o in ambienti di lavoro ove è prescritto l’uso di specifici DPI. A rigore, andranno inoltre riportate tutte le altre informazioni a tutela del consumatore previste dal Codice del Consumo (sul punto sono interessanti anche l’Ordinanza n. 9/2020 del Commissario Straordinario e la Circolare MISE 107886 del 23.4.2006). |
Come controllare la certificazione di un DPI
Anzitutto va precisato che ogni DPI marcato CE deve fare capo (quindi possedere quindi deve essere disponibile e consultabile dall’utente) una dichiarazione di conformità ai sensi Regolamento UE 425/2016. La dichiarazione di conformità comunemente chiamata certificazione, deve contenere almeno le seguenti informazioni:
a) nome e numero di identificazione dell’organismo notificato;
b) nome e indirizzo del fabbricante e, qualora la domanda sia presentata dal mandatario, nome e indirizzo di quest’ultimo;
c) identificazione del DPI oggetto del certificato (numero del Tipo);
d) dichiarazione in cui si attesta che il Tipo di DPI soddisfa i requisiti essenziali di salute e di sicurezza applicabili;
e) se le norme armonizzate sono state applicate in tutto o in parte, i riferimenti di tali norme o parti di esse;
f) se sono state applicate altre specifiche tecniche, i loro riferimenti;
g) se del caso, il livello di prestazioni o la classe di protezione del DPI;
h) per i DPI prodotti come unità singole per adattarsi a un singolo utilizzatore, la gamma delle variazioni consentite dei parametri pertinenti sulla base del modello di base approvato;
i) la data di rilascio, la data di scadenza e, se del caso, la data o le date di rinnovo;
j) le eventuali condizioni connesse al rilascio del certificato;
k) per i DPI della categoria III, una dichiarazione secondo cui il certificato deve essere utilizzato solo in combinazione con una delle procedure di valutazione della conformità di cui all’articolo 19, lettera c).
NOTA BENE: le informazioni di cui ai punti e), f), g), h) potrebbero anche non essere sempre presenti in base alle scelte progettuali e costruttive dei diversi fabbricanti.
Particolare attenzione deve essere osservata al punto (a). Per essere certi che il certificato che contiene gli elementi sopra riportati sia stato emesso da un organismo notificato per tale tipologia di DPI, si può effettuare un controllo sul database della Commissione europea che riporta l’elenco degli organismi notificati in Europa per il Regolamento UE 425/2016.
LINK –> Database NANDO
Bisogna verificare se nella specifica notifica è riportato il DPI oggetto della ricerca (Equipment providing respiratory system protection).
Come detto sopra, in questo periodo di emergenza è possibile che – benché non marcati CE – alcuni DPI siano immessi in commercio in forza di quanto previsto dall’art. 15 del DL 18/2020 “Cura Italia”. L’elenco di tali DPI è pubblico e consultabile sul sito di INAIL.
Qualora il DPI oggetto di approfondimento non dovesse risultare correttamente marcato CE e non “validato” da INAIL, è possibile segnalarlo alle Autorità preposte alla Sorveglianza del mercato. Per i DPI le segnalazioni vanno inviate al Ministero dello Sviluppo Economico e al Ministero del Lavoro e delle Politiche Sociali agli indirizzi pubblicati sui relativi siti.
Per i Dispositivi Medici (mascherine chirurgiche) si specifica che le Autorità preposte alla Sorveglianza del mercato sono il Ministero della Salute e l’Istituto Superiore di Sanità.
ATTENZIONE ALLE FALSE ATTESTAZIONI !!!

Come indicato sul sito di Accredia (associazione riconosciuta che opera senza scopo di lucro, sotto la vigilanza del Ministero dello Sviluppo Economico), stanno circolando documenti simili a dei certificati del Tipo di DPI ai sensi del Regolamento UE 425/2016 DPI ma che non lo sono.
Diciture generiche sui facsimili di certificati presentati a supporto di DPI del tipo FFP2 e FFP3 che contengano diciture come “Qualified Certificate”, “Protective Mask” o “Contrasto COVID-19” non sono previste dalla legislazione vigente e anzi rappresentano un elemento che può confondere i consumatori finali e di cui bisogna diffidare ponendo la massima attenzione alla reale conformità del DPI che viene proposto.
Per ulteriori approfondimenti sulla deprecabile commercializzazione fraudolenta delle mascherine, consultare anche questo link
Conclusioni
La consapevolezza del delicato periodo di pandemia che stiamo attraversando, dell’importanza dell’efficacia dei sistemi di protezione unitamente all’oggettiva rilevanza che possono assumere comportamenti scorretti sul mercato, ci mettono in condizione di sconsigliare e diffidare chiunque intenda produrre e commercializzare (o regalare) questo tipo di sistemi a terzi senza aver validato gli stessi secondo i metodi previsti dalle leggi.
Questi sistemi sono oggetto di verifiche ben precise proprio per tutelare l’incolumità di chi le utilizza in queste condizioni. Suggeriamo agli utilizzatori di prestare la massima attenzione e verificare che ciò che indossiamo per proteggerci abbia un efficacia validata da enti preposti ed indipendenti. La salute è un bene prezioso pertanto è bene non dare nulla per scontato.